磁驱动机器人胶囊内镜的设计与研发 —— 胃肠道原位可视化及微针介导靶向给药研究

一、研究背景
胃肠道疾病发病率高、致死率可观,传统胃镜等侵入式诊断手段易引发患者不适,而 1995 年提出、2000 年临床应用的胶囊内镜虽实现无创成像诊断,却仅具备单一诊断功能,无法同步开展治疗,后续需额外侵入式操作,增加诊疗复杂度与患者痛苦。科研人员虽尝试将机器人技术与胶囊内镜结合开发机器人胶囊内镜,并融入磁驱动、微针给药等技术,但现有产品仍存在诸多缺陷:部分缺乏主动移动能力,无法实现病灶精准靶向给药;部分仅具备治疗功能,无视频诊断反馈;微针给药类产品也存在靶向精度不足、无法兼顾诊断与治疗的问题,临床亟需一款集精准导航、原位可视化、靶向治疗于一体的胶囊内镜产品。
二、研究目标
研发一款磁驱动机器人胶囊内镜(MARCE),突破传统胶囊内镜 “仅诊不治”、现有机器人胶囊内镜 “诊疗分离” 的技术瓶颈,实现胃肠道内磁控精准导航、实时原位可视化观察与微针介导的多靶点精准给药一体化,为胃肠道疾病提供微创、高效、精准的诊疗一体化解决方案,提升患者诊疗舒适度与治疗精准度。
三、创新点
功能集成创新:首次实现磁控导航、可伸缩微型相机原位可视化、双层透明质酸微针靶向给药三大功能的高度集成,打造了胃肠道诊疗一体化的胶囊内镜平台,解决了现有产品诊疗分离的核心问题。
结构设计创新:①设计磁弹簧驱动的可伸缩微型相机,避免相机遮挡微针穿刺,且实现视野动态调整,保障原位观察的连续性;②研发电热触发的防护盖结构,外层聚四氟乙烯涂层可防止微针在胃肠道内提前溶蚀,内层可溶性基材在触发后快速溶解,保障微针给药的时效性与有效性;③设计双层微针贴片结构,可实现胃肠道多病灶的依次精准给药,满足临床多靶点治疗需求。
磁驱动技术创新:自主研发正交式麦克斯韦 - 亥姆霍兹线圈电磁驱动(EMA)系统,可提供 0.58 N 的磁驱动力与 18.4 N・mm 的磁扭矩,实现胶囊内镜三维空间的精准移动与姿态调整,平均定位误差<1.5 mm,微针穿刺定位误差低至 1.36~1.43 mm,满足胃肠道内精准导航与给药要求。
安全与性能创新:①电热触发防护盖的最优工作电压为 2.2 V,响应延迟仅 1.07 s,且触发后温度变化控制在 1.5 ℃内,无胃肠道组织热损伤风险;②微针贴片最大穿刺力仅 0.15 N,可实现胃肠道黏膜层安全穿刺,且透明质酸微针可快速溶蚀,单次最大给药量达 0.4 mg,匹配临床肾上腺素止血的剂量需求;③胶囊内镜尺寸为 11.8 mm(直径)×21.5 mm(长度),与临床常规胶囊内镜一致,具备临床转化的硬件基础。
四、研究结论与意义
研究结论
:研发的磁驱动机器人胶囊内镜(MARCE)在结构与性能上均达到临床应用的核心要求,其尺寸与商用胶囊内镜兼容,经离体猪肠组织实验验证,可实现胃肠道内平均<1.5 mm 的精准磁控导航,通过可伸缩相机完成病灶原位可视化观察,借助电热触发防护盖与双层微针贴片,实现黏膜层安全穿刺与多病灶靶向给药,微针可快速溶蚀并释放药物,且整个诊疗过程无热损伤、穿刺损伤等安全风险,诊疗一体化的功能与性能均得到有效验证。
研究意义
:①技术层面,突破了胶囊内镜诊疗分离、磁驱动导航精度低、微针给药易提前失效等关键技术瓶颈,为机器人胶囊内镜的研发提供了新的结构设计与技术思路;②临床层面,打造了胃肠道疾病的微创诊疗一体化平台,无需额外侵入式操作,大幅降低诊疗复杂度,提升患者舒适度,同时实现病灶的精准定位与靶向给药,提高治疗精准度,为胃肠道出血、炎症、溃疡等疾病的治疗提供了新的微创方案;③应用层面,胶囊内镜的尺寸兼容性、磁驱动系统的可控性与操作的便捷性,使其具备良好的临床转化潜力,有望推动胶囊内镜从 “诊断工具” 向 “诊疗一体化工具” 的升级。
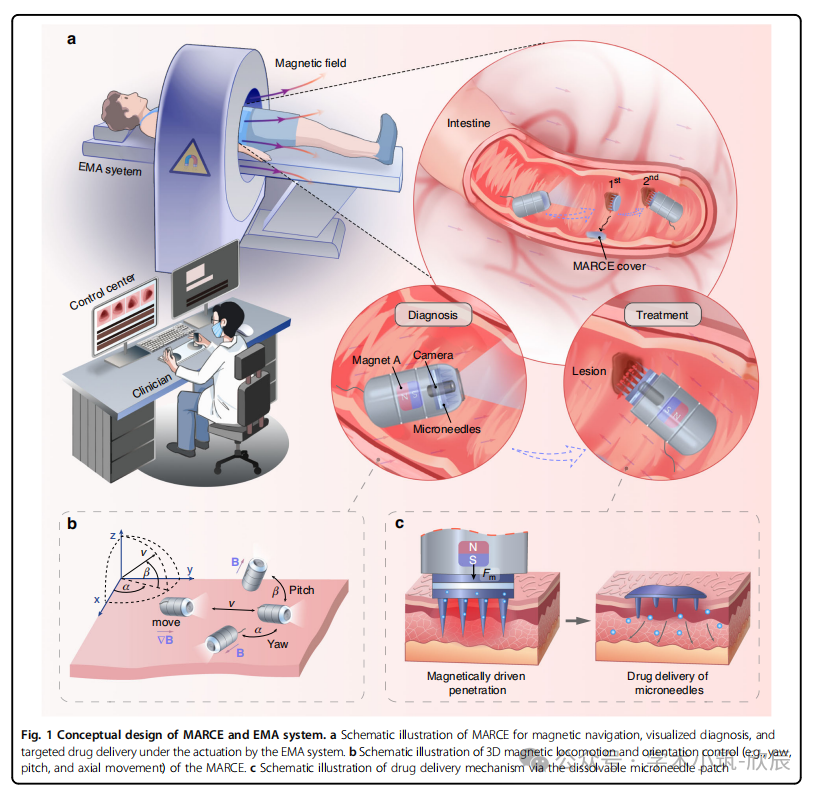
图1 MARCE与EMA系统的概念设计。a) 示意图展示MARCE在EMA系统驱动下,实现磁导航、可视化诊断与靶向给药的综合功能。b) 示意图展示MARCE的三维磁控运动与定向控制(例如偏航、俯仰及轴向移动)。c) 示意图展示通过可溶解微针贴片实现给药的机制。
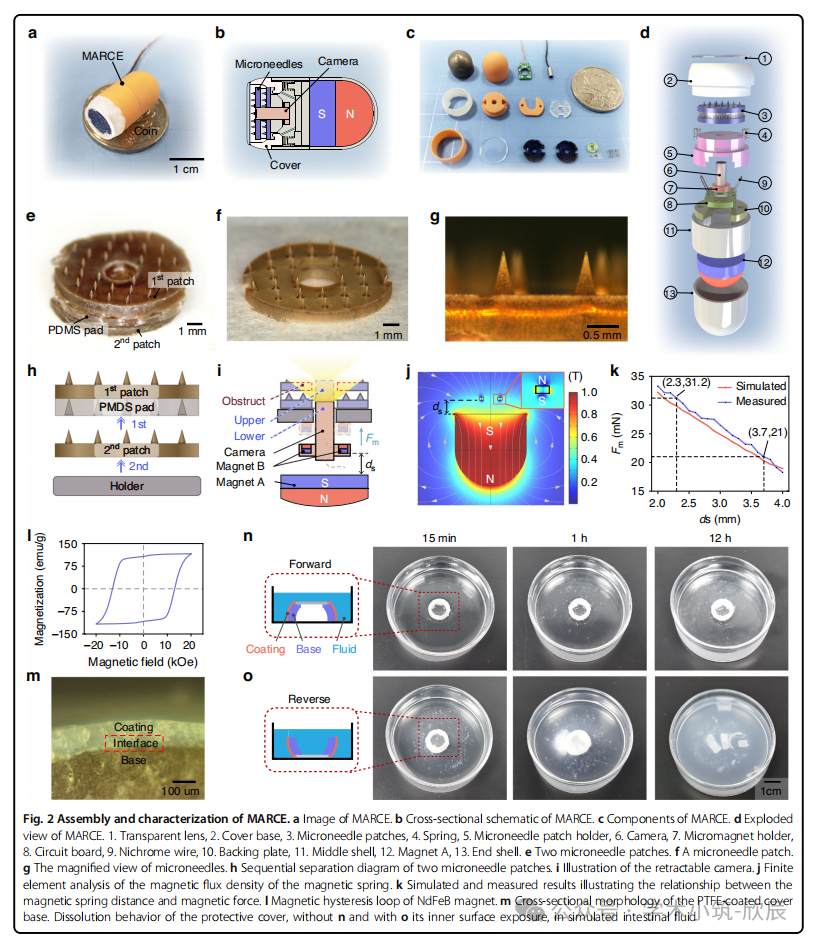
图2 MARCE的组装与表征。a) MARCE的整体图像。b) MARCE的横截面示意图。c) MARCE的组成部件。d) MARCE的爆炸视图。1. 透明透镜,2. 覆盖基座,3. 微针贴片,4. 弹簧,5. 微针贴片支架,6. 摄像头,7. 微磁体支架,8. 电路板,9. 镍铬合金线,10. 背板,11. 中间壳体,12. 磁体A,13. 端部壳体。e) 两个微针贴片。f) 单个微针贴片。g) 微针的放大视图。h) 两个微针贴片的顺序分离示意图。i) 可伸缩摄像头的示意图。j) 磁弹簧磁通量密度的有限元分析。k) 展示磁弹簧距离与磁力关系的模拟与测量结果。l) 钕铁硼磁体的磁滞回线。m) PTFE涂层覆盖基座的截面形貌。保护罩在模拟肠液中的溶解行为:n) 内表面未暴露时;o) 内表面暴露时。
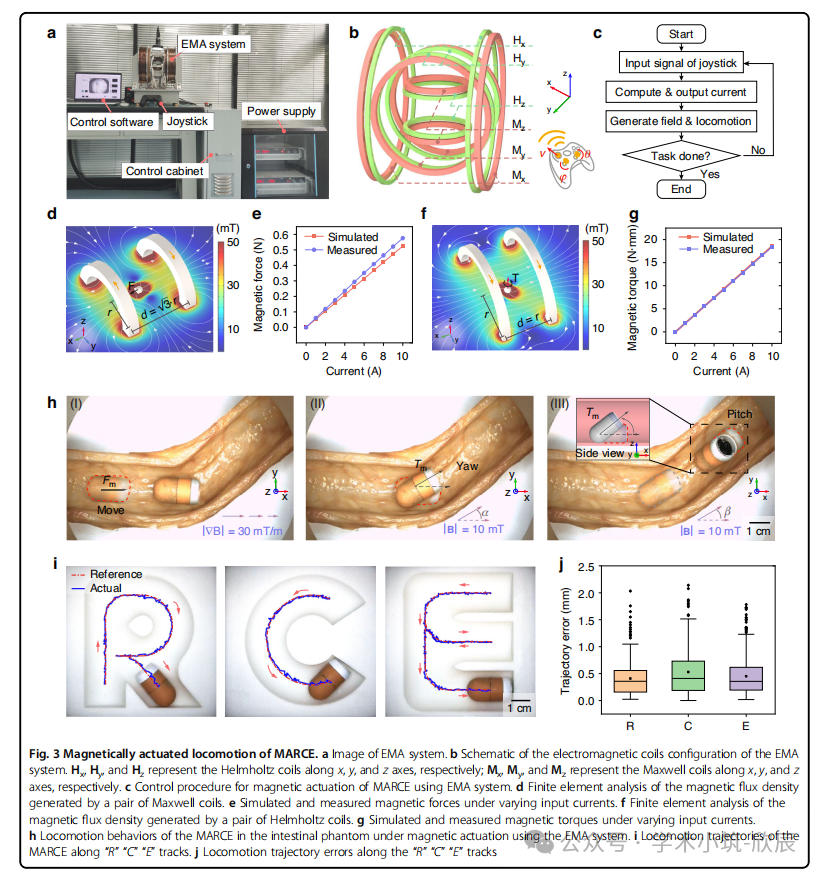
图3 MARCE的磁控运动。a) EMA系统的图像。b) EMA系统电磁线圈配置示意图。Hx、Hy和Hz分别代表沿x、y、z轴的亥姆霍兹线圈;Mx、My和Mz分别代表沿x、y、z轴的麦克斯韦线圈。c) 使用EMA系统对MARCE进行磁力驱动的控制流程。d) 一对麦克斯韦线圈产生的磁通量密度的有限元分析。e) 不同输入电流下的模拟与实测磁力。f) 一对亥姆霍兹线圈产生的磁通量密度的有限元分析。g) 不同输入电流下的模拟与实测磁矩。h) MARCE在肠体模中使用EMA系统进行磁力驱动时的运动行为。i) MARCE沿"R"、"C"、"E"路径的运动轨迹。j) 沿"R"、"C"、"E"路径的运动轨迹误差。
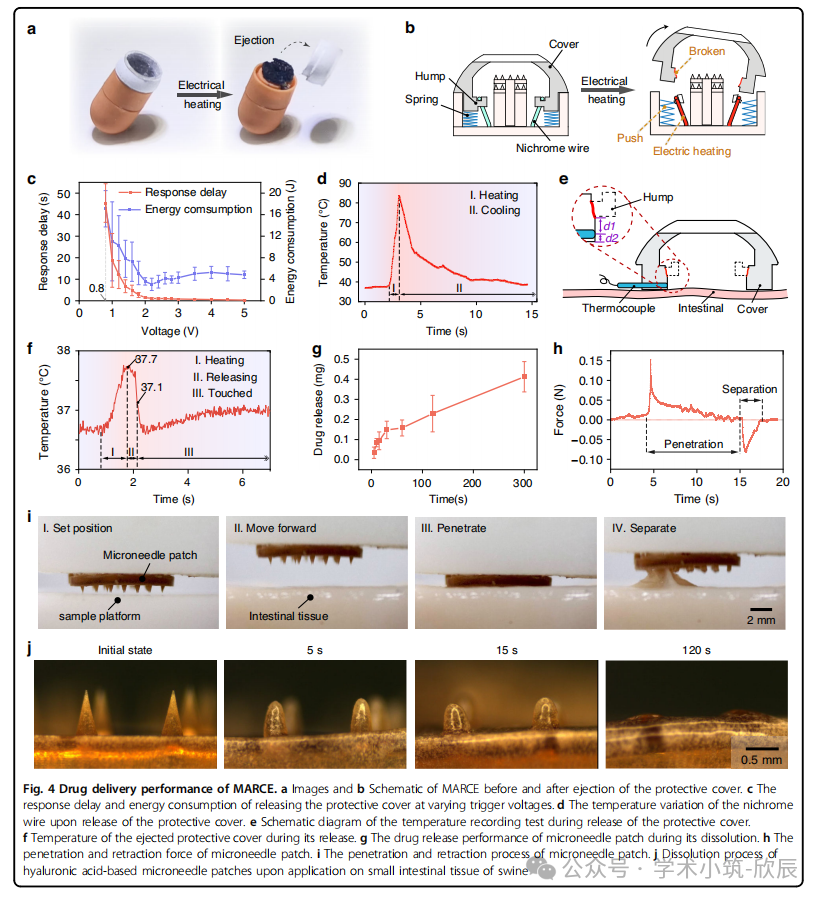
图4 MARCE的药物递送性能。a) 图像与 b) 示意图展示弹射保护罩前、后的MARCE。c) 在不同触发电压下,释放保护罩的响应延迟与能量消耗。d) 释放保护罩时镍铬合金线的温度变化。e) 释放保护罩过程中的温度记录测试示意图。f) 弹射出的保护罩在释放过程中的温度。g) 微针贴片在溶解过程中的药物释放性能。h) 微针贴片的刺入力与拔出力。i) 微针贴片的刺入与拔出过程。j) 基于透明质酸的微针贴片在猪小肠组织上使用时的溶解过程。
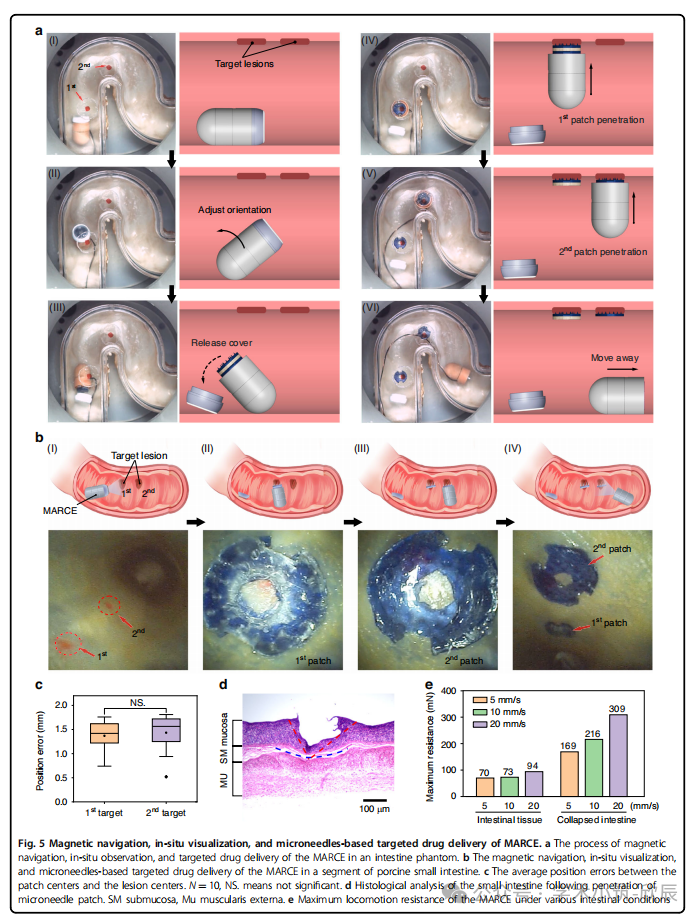
图5 MARCE的磁导航、原位可视化与基于微针的靶向药物递送。a) MARCE在肠道模型中进行磁导航、原位观察及靶向药物递送的过程。b) MARCE在一段猪小肠中进行磁导航、原位可视化及基于微针的靶向药物递送。c) 贴片中心与病灶中心之间的平均位置误差。N = 10,NS. 表示不显著。d) 微针贴片刺入后小肠的组织学分析。SM:黏膜下层,Mu:外肌层。e) MARCE在不同肠道状态下的最大运动阻力。
全文转自:https://mp.weixin.qq.com/s/-P8Uclb__qDSNUFncbaHtA


