王佳力副教授课题组在可降解镁基骨科植入物研究方面发表重要综述
可降解镁基金属骨科植入物由于力学模量适中且降解产物可促骨再生,近年来已成为基础研究和临床转化应用研究热点。当前,镁基骨科器械的研发仍存在镁降解过快及力学强度不足等制约因素,限制其临床应用,尤其在承重部位骨的固定修复。现有骨科植入器械对难治愈骨相关疾病,如骨质疏松性骨折、长期使用抗骨质疏松药物二磷酸盐后出现的非典型股骨骨折和股骨头坏死,临床治疗效果并不理想。开发兼具生物学效应和足够的力学强度的含镁骨科器械,是决定能否将其规模化推向临床多种应用的关键。
最近,Advanced Science在线发表了中山大学生物医学工程学院王佳力副教授与香港中文大学医学院骨科秦岭教授联合工作:“可降解镁基骨科植入物发展、挑战与展望”(Wang JL et al. Biodegradable Magnesium-Based Implants in Orthopaedics-A General Review and Perspectives. Advanced Science, 2020, 1902443)。文章针对性地提出了三个重要策略:
(1)材料表面改性,如表面机械研磨与涂层沉积联用(Surface Mechanical Attribution Treatment & Coating Deposition),改善镁金属抗腐蚀性能和力学强度(图1);
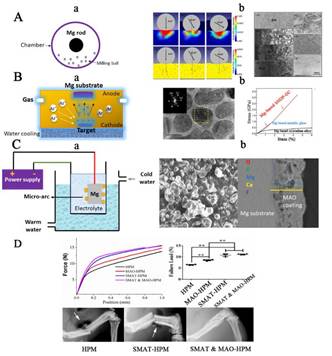
图1 镁金属表面改性技术改善抗腐蚀性能和力学性能
(2)注射活性生物材料和植入器械组合,形成镁离子/药物(如中药活性组分)离子协同效应,促进难治愈骨疾病中股骨头坏死的治疗和新骨生成(图2)。
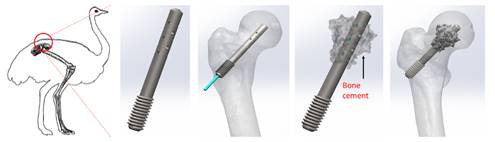
图2 药(生物活性因子缓释)械(镁骨科器械)组合
(3)含镁组合器械联用,分别发挥镁离子的生物学效应和惰性金属力学强度优势,应用于高承力部位如骨质疏松性骨折等的骨损伤修复(图3)。
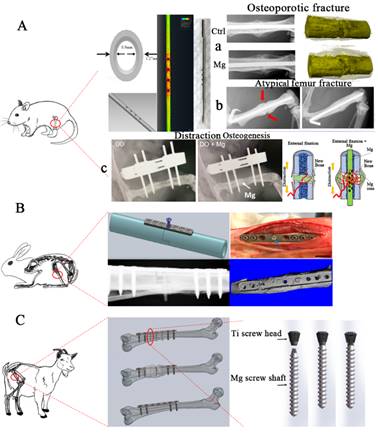
图3 含镁组合器械应用于高承力部位固定修复骨损伤
此外,文章还总结概括了镁离子的生物学效应,从加强感觉神经-骨膜干细胞对话、促进血管新生、免疫性调节成骨分化和抑制破骨分化融合等多个角度阐释了镁离子在骨损伤修复中的作用机制(图4),为镁基骨科器械的临床应用提供科学佐证。
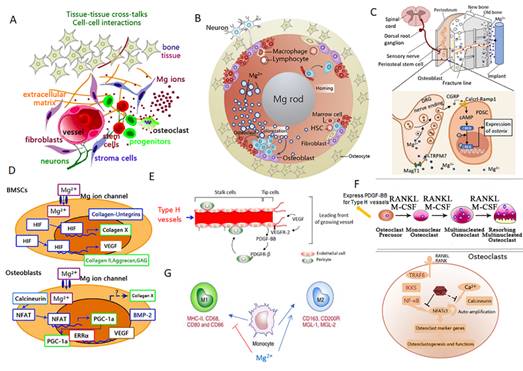
图4 镁离子生物学效应产生机制
中山大学王佳力副教授是本文的第一作者兼通讯作者,香港中文大学许建坤研究助理教授是共同第一作者,香港中文大学秦岭教授是共同通讯作者。本论文是基于发表在Nature Medicine (2016, 22:1160)、Biomaterials (2018, 157:86;2017, 112:287)和Acta Biomaterialia(2017, 63:393; 2015, 21:237)等系列基础研究和临床科研工作的总结与展望,将为镁基骨科器械的研发与临床应用提供更多的策略。
论文地址:https://onlinelibrary.wiley.com/doi/full/10.1002/advs.201902443

